Introduction
L’examen échographique est la technique d’imagerie la plus pratiquée [1] en raison de sa disponibilité, de l’absence de danger perçu pour les patients, et d’un coût maîtrisé. Se pose la problématique de l’asepsie des sondes d’échographie réutilisables, en particulier lorsqu’il s’agit d’examens endocavitaires [2,3]. Le risque infectieux associé est lié à la fois à la qualité des pratiques d’hygiène qui entourent le geste (hygiène des mains, entretien de l’environnement et gel d’échographie) et à la gestion des sondes endocavitaires elles-mêmes [4,5,6]. Les sondes d’échographie endocavitaire (SEE) (transœsophagiennes, endovaginales et endorectales) peuvent être en contact avec des muqueuses en cas de non-utilisation d’une gaine à usage unique ou de perte d’étanchéité de celle-ci. Du point de vue du risque infectieux, il s’agit de dispositifs médicaux (DM) semi-critiques selon la classification de Spaulding [7] et de classe IIb selon le Guide de bonnes pratiques de traitement des dispositifs médicaux réutilisables de la Société française d’hygiène hospitalière (SF2H) de 2022 [8]. En fonction des gestes associés, des souillures par du sang ou d’autres liquides biologiques sont plus ou moins fréquemment constatées, avec un risque de contamination par des micro-organismes [9]. L’analyse de risque viral hématogène, réalisée dans les conditions des recommandations du Haut Conseil de la santé publique (HCSP) de 2007 [10] et 2008 [11], n’a pas permis d’identifier l’échographie endocavitaire, sur d’importantes cohortes rétrospectives, comme un geste présentant un risque de contamination par les virus VHC et VIH1 [12]. Pour le risque lié aux virus HPV2 et dans le doute, il doit être intégré dans la réflexion concernant la désinfection [13]. Les micro-organismes ainsi transmis sont responsables d’infections associées aux soins comme cela a été le cas avec du gel [14] et des sondes d’échographie [15]. Dans une revue systématique de sept études sur les infections liées à des sondes échographiques contaminées, l’auteur a montré que les infections étaient liées à une défaillance du processus de décontamination des appareils à ultrasons utilisés [16]. L’analyse des cas montre des liens entre les épidémies d’infection et la contamination de l’environnement, le manque de processus normalisés de désinfection des sondes à ultrasons, un stockage inadéquat et le manque de surveillance de l’intégrité des sondes. La mise en place de mesures d’hygiène renforcées permet donc de réduire les infections associées aux soins en réduisant la transmission croisée. Le HCSP a proposé des recommandations à trois reprises en 2007, 2008 et 2016 sur le sujet de la désinfection des SEE [17]. Une instruction du 10 mai 2016 relative aux échographies endocavitaires [18] a ainsi rappelé, pour la première fois, « aux professionnels de santé pratiquant des échographies endocavitaires l’impératif de respecter les recommandations en vigueur du Haut Conseil de la santé publique (2007, 2008) ». Cette instruction précisait également « que la systématisation d’une désinfection de niveau intermédiaire entre chaque patient est de nature à prévenir la transmission des contaminants liés aux liquides biologiques lors des actes d’échographie endocavitaire ». Dans ce cadre, en avril 2017, la SF2H a été missionnée afin de faire le point sur les pratiques professionnelles, les recommandations existantes et les procédés de désinfection disponibles. À l’issue de cette réflexion, un guide de recommandations composé de neuf fiches techniques relatives à la prévention du risque infectieux associé aux actes d’échographie endocavitaire a été élaboré [19]. Ces fiches précisent les situations pour lesquelles une désinfection de niveau intermédiaire (DNI) est préconisée, soit par des procédés automatisés, soit par des lingettes désinfectantes virucides, et proposent des recommandations aux professionnels de santé sur les procédés de désinfection des sondes. Elles s’appuient sur l’évolution des connaissances scientifiques et sur les innovations techniques disponibles. Les enquêtes de pratiques, tant françaises qu’européennes, montrent une faible adhésion aux recommandations en vigueur avec des niveaux de qualité ne pouvant garantir la sécurité des patients vis-à-vis du risque infectieux dans son ensemble [20,21,22,23,24,25]. Avec la diffusion en 2019 des recommandations nationales, les SEE ont été classées pour la première fois comme des DM devant subir une désinfection de niveau intermédiaire au lieu d’une désinfection de bas niveau. Ce changement de paradigme a conduit à la réalisation d’une enquête documentaire et d’un audit de pratiques pour évaluer le risque de contamination. Le groupe de travail commun aux centres d’appui pour la prévention des infections associées aux soins (inter-CPias) a donc proposé, fin 2021, un premier audit à tous les établissements de santé (ES) français qui réalisaient des échographies avec SEE (transœsophagiennes, endovaginales et endorectales). L’enquête s’est appuyée sur les neuf fiches techniques relatives à la prévention du risque infectieux associé aux actes d’échographie endocavitaire de mars 2019 [19], sous forme d’un audit documentaire déclaratif pour évaluer les procédures. Cet audit interrégional, auquel ont participé 240 ES de 17 régions, a conclu à l’existence d’incertitudes concernant l’appropriation des recommandations nationales de 2019 [26]. Compte tenu des résultats non concluants de l’audit déclaratif de 2022, l’inter-CPias a souhaité poursuivre en 2023 l’exploration des procédures de nettoyage et de désinfection des SEE. Cette fois-ci, un quick audit d’observation a été proposé, méthode plus précise qu’un audit documentaire. Cet article en rapporte les principaux résultats.
Méthodes et outil de travail
Le quick audit mené en 2023 avait pour objectif d’évaluer la conformité des pratiques de nettoyage et de désinfection des SEE dans les ES par rapport au référentiel Prévention du risque infectieux associé aux actes d’échographie endocavitaire, publié par la SF2H en mars 2019. L’enquête s’est appuyée sur les neuf fiches techniques relatives à la prévention du risque infectieux associé aux actes d’échographie endocavitaire diffusées en mars 2019 [19] ainsi que sur la note d’information no 79 du 19 juillet 2019 relative à la désinfection des sondes endocavitaires3 qui avait été adressée aux agences régionales de santé. Le Guide de bonnes pratiques de traitement des dispositifs médicaux réutilisables publié par la SF2H en novembre 20224 a également servi de base à l’élaboration de cette enquête. L’audit proposé était un quick audit mixte, composé d’une part d’observations des pratiques de nettoyage et de désinfection des SEE et d’autre part d’une auto-évaluation des freins aux bonnes pratiques des professionnels. Il a été réalisé de septembre à décembre 2023 auprès des professionnels des ES avec une activité de prise en charge du nettoyage et de la désinfection des SEE de manière régulière ou occasionnelle. Les données ont été recueillies à l’aide de trois fiches d’observation à renseigner selon la méthode de désinfection utilisée (par essuyage, par immersion ou par automate) et d’un questionnaire permettant d’identifier les freins à la mise en œuvre de pratiques conformes aux recommandations. Ces fiches ont été renseignées et leurs données saisies sur un outil en ligne par les équipes opérationnelles d’hygiène des établissements participants. Les analyses statistiques ont été réalisées à l’aide du logiciel SAS© version 9.4 (SAS Institute Inc., Cary, NC, États-Unis).
Résultats
Participation
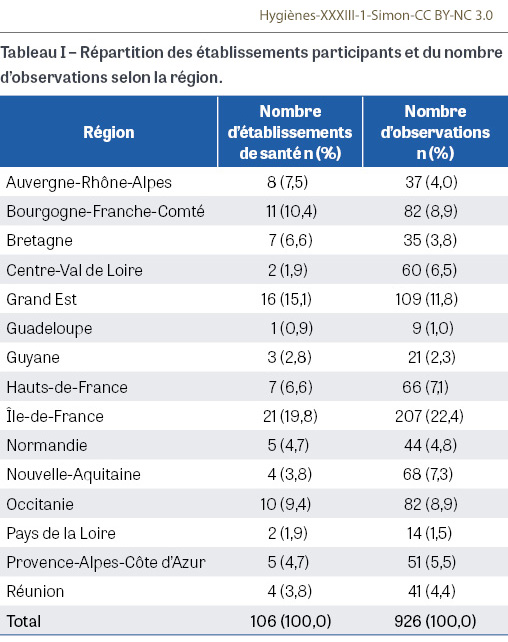
Cet audit a été proposé à tous les ES français sur la base du volontariat avec le soutien des CPias de chaque région de France. En pratique, 15 régions ont participé sur les 18 existantes soit un taux de participation de 83,3%. Le nombre d’établissements participants par région a été très variable (Tableau I). Le nombre total de retours est resté faible (106) et variable d’une région à l’autre par rapport au nombre d’ES sollicités ; 926 observations ont été recueillies.
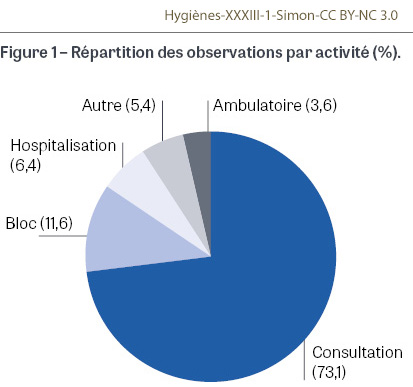
Les activités et les spécialités concernées par l’échographie endocavitaire
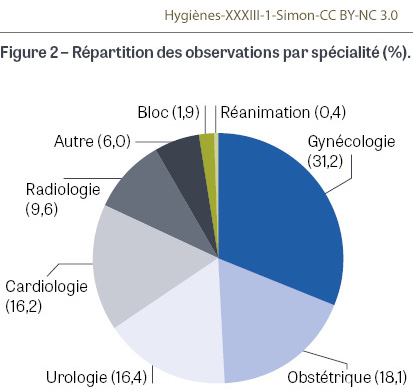
Les échographies endocavitaires sont réalisées majoritairement dans les services de consultation, qui représentent 73,1% des observations (n=677) (Figure 1). La gynécologie-obstétrique est la spécialité pour laquelle ont été réalisées le plus d’observations (49,3%), vient ensuite l’urologie (16,4%), suivie de près par la cardiologie (16,2%) (Figure 2).
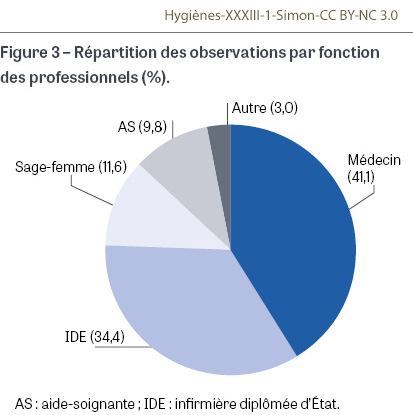
Les professionnels concernés par l’échographie endocavitaire
Les professionnels les plus représentés dans cet audit (Figure 3) sont les médecins (41,1%), suivis des infirmières (34,4%). En troisième position, les sages-femmes représentent 11,6% des professionnels observés.
Répartition par méthode de désinfection des sondes d’échographie endocavitaires
La méthode de désinfection par essuyage est la plus utilisée (76,8% soit 711 observations), loin devant la méthode de désinfection par automate (15,4% soit 143 observations). La méthode de désinfection par immersion est la moins pratiquée (7,8% soit 72 observations).
Comparaison des pratiques communes aux trois méthodes de désinfection
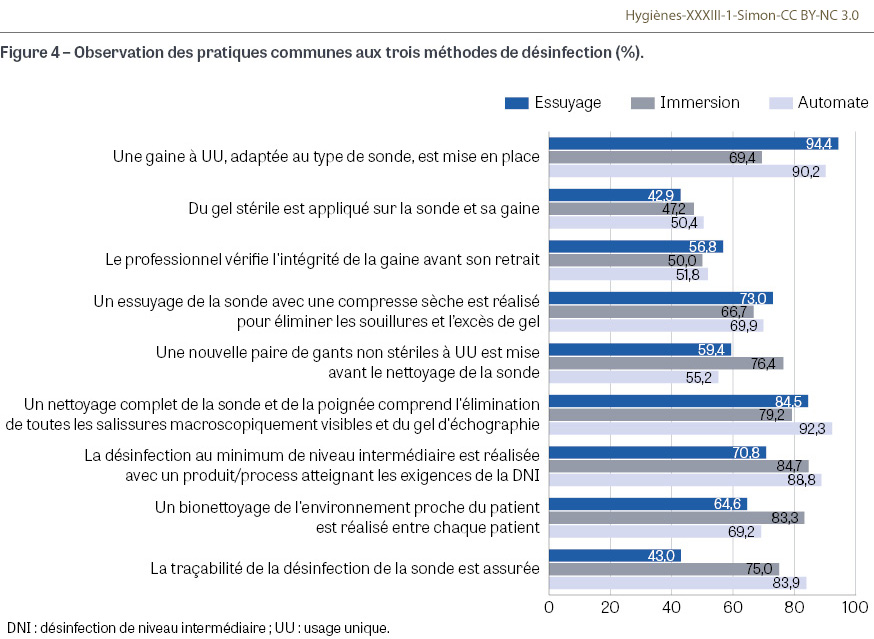
L’observation des étapes identiques des processus des trois méthodes de désinfection (Figure 4) dévoile des résultats de conformité parfois hétérogènes dans le traitement et la désinfection des SEE. L’utilisation d’une gaine à usage unique adaptée à la forme de la sonde est respectée dans plus de 90,0% des cas, sauf pour les professionnels utilisant la méthode de désinfection par immersion, qui n’atteignent que 69,4% de conformité. Cette méthode par immersion ne dispense pas de l’utilisation d’une gaine à usage unique adaptée. Du gel stérile en conditionnement individuel devrait obligatoirement être utilisé pour les examens semi-critiques et critiques mettant en contact le transducteur avec une muqueuse. Or moins de 50,0% des professionnels observés utilisent un gel stérile sur la sonde et sur la gaine. Une analyse par spécialité montre qu’en gynécologie-obstétrique l’application de gel stérile sur la sonde et sa gaine n’est réalisée que dans 31,9% des cas, alors qu’en urologie et cardiologie elle est réalisée dans respectivement 71,1% et 62,0% des cas. L’étape de vérification de l’intégrité de la gaine après examen et avant son retrait n’apparaît que très peu intégrée dans les pratiques professionnelles, quelle que soit la méthode de désinfection utilisée. Seulement un peu plus de la moitié des professionnels observés procède à ce contrôle. Le changement de gants à usage unique avant le nettoyage de la sonde est peu réalisé pour l’ensemble des professionnels observés (moins de 60,0%), sauf pour la méthode par immersion, où les professionnels changent de gants dans 76,4% des cas. C’est en gynécologie-obstétrique que le changement de gants est le moins réalisé (44,0%), comparé à l’urologie (77,0%) et la cardiologie (83,3%). Plus de 85,0% des professionnels observés réalisent un nettoyage complet de la sonde et sa poignée. La nécessité d’une DNI au minimum avec un produit ou un processus adapté, est respectée par plus de 85,0% des professionnels, principalement les pratiquants des méthodes de désinfection par immersion et par automate. Les utilisateurs de la méthode de désinfection par essuyage avec des lingettes semblent moins respecter ces exigences (70,8%). L’analyse par spécialité montre que ces exigences sont moins respectées en gynécologie-obstétrique (65,2%) qu’en urologie (82,9%) et en cardiologie (87,3%). L’étape du bionettoyage de l’environnement proche du patient entre chaque examen pour toutes les observations réalisées n’est étonnamment pas acquise car non réalisée dans 30,0% des observations. La traçabilité est mieux assurée dès lors qu’un automate est utilisé, du fait de la présence d’un enregistrement du processus intégré à l’automate, et moins réalisée lors de la méthode par essuyage.
Analyse des observations par méthode de désinfection
Comme vu précédemment, la désinfection par essuyage est la méthode la plus pratiquée (n=711/926) et l’analyse des résultats montre qu’en cas de rupture de la gaine seulement 44,3% des ES participants possèdent une procédure écrite par immersion. Une méconnaissance du type de lingettes DNI recommandé, à savoir de classe IIb, est également confirmée par le résultat obtenu chez 31,4% des professionnels. Le temps de séchage permettant une action complète du produit de désinfection est, quant à lui, une étape comprise et respectée par la majorité des professionnels observés (89,2%). Pour la méthode de désinfection par immersion, le nettoyage complet, la phase de rinçage et l’immersion dans un produit atteignant les exigences de la DNI semblent respectés par 80,6% des professionnels observés. Mais l’utilisation d’une eau bactériologiquement maîtrisée pour la phase de rinçage final n’est respectée que dans 59,7% des cas observés. L’air médical recommandé pour l’étape de séchage de la sonde et de sa poignée est très peu utilisé (25,0%), probablement parce qu’il est indisponible dans les services de consultation. Les observations de la méthode de désinfection par automate révèlent quant à elles, qu’à la fin de l’examen, en cas de rupture de la gaine, seulement 35,7% des professionnels disposent d’une procédure écrite de désinfection par immersion dans leur établissement. Les produits ou processus utilisés pour cette méthode de désinfection atteignent le niveau d’exigence de DNI pour 88,8% des professionnels observés.
Freins à la bonne réalisation de l’entretien des sondes d’échographie endocavitaires
Un questionnaire d’identification des freins a été complété par 516 professionnels observés, essentiellement des médecins et des sages-femmes. Plus d’un tiers de ces professionnels n’identifient pas de frein au respect de la procédure. Pour les deux autres tiers, le manque de formation à la technique, le manque de matériel ou le manque d’information sur la procédure étaient les trois principaux freins revendiqués. Le manque de temps entre chaque examen est également rapporté par 17,6% des professionnels comme obstacle au respect de la procédure.
Discussion
Après les résultats non concluants d’un premier audit déclaratif sur les procédures de désinfection des SEE en août 2022, qui faisait suite aux recommandations nationales de mars 2019 [26], cette nouvelle enquête a été menée en 2023 sous la forme d’un quick audit observationnel sur les pratiques de désinfection des SEE. Elle a permis de recueillir 926 observations malgré le nombre réduit d’établissements participants (106 ES), répartis dans la majorité des régions françaises [27]. L’échographie endocavitaire est surtout réalisée dans les services de consultation, en particulier les services de gynécologie-obstétrique. La désinfection par essuyage avec des lingettes est la méthode majoritairement utilisée dans les établissements, suivie par la désinfection par automate. La désinfection par immersion est très peu utilisée. Les recommandations de la SF2H concernant la mise à disposition d’une gaine à usage unique adaptée à la forme des SEE pour la méthode par essuyage et par automate sont respectées. Ce n’est pas le cas dans les établissements utilisant la méthode par immersion, ces derniers s’en sentant peut-être exemptés. Or la recommandation de mettre à disposition des gaines à usage unique adaptées à la forme de la sonde s’applique quelle que soit la méthode de désinfection pratiquée. À la fin de l’examen, la vérification de l’intégrité de la gaine avant son retrait est acquise par trop peu de professionnels, quelle que soit la méthode de désinfection des SEE. Pour rappel, en cas de rupture de la gaine en fin d’examen, un nombre conséquent d’établissements qui utilisent la méthode de désinfection par essuyage et la méthode par automate ne possèdent pas de procédure décrivant une désinfection par immersion, comme recommandé dans la foire aux questions de la SF2H [28]. L’utilisation systématique de gel stérile en conditionnement individuel pour ces examens semi-critiques et critiques n’est toujours pas respectée alors que la fiche 6 du guide de 2019 la rappelle [19]. Si l’utilisation de produits ou processus respectant les exigences normatives de la DNI pour les méthodes de désinfection par immersion et par automate semble respectée, il est indispensable que les utilisateurs améliorent leur connaissance des différentes classes de lingettes. En effet, selon le nouveau règlement européen 2017/745 relatif aux dispositifs médicaux, qui est entré en application le 26 mai 2021, seules les lingettes de classe IIb sont désormais requises pour la désinfection des dispositifs invasifs comme les sondes endocavitaires. C’est une évolution importante pour renforcer la sécurité des dispositifs médicaux en termes de prévention du risque infectieux dans l’intérêt des patients [29]. Le bionettoyage de l’environnement proche du patient entre deux examens reste non acquis pour un ensemble de professionnels, alors qu’il fait partie intégrante des précautions standard, qui doivent être respectées par tout professionnel de santé, et qu’il avait été rappelé dans l’étude de Lucet [30]. Enfin la traçabilité des procédés de nettoyage, désinfection et (ou) stérilisation n’est pas réalisée sauf quand elle est automatisée, avec une fonction intégrée dans l’équipement médical, alors qu’elle est recommandée et rappelée dans le guide de la SF2H de 2022 [8]. Les résultats de notre enquête sont proches de l’enquête européenne pilotée par la Société européenne de radiologie réalisée en 2016 [31], qui montrait déjà un large éventail des pratiques dans toute l’Europe et la nécessité de sensibiliser les praticiens à l’importance des mesures de prévention et de contrôle des infections. À l’époque, des recommandations européennes étaient en cours d’élaboration, alors qu’aujourd’hui ces recommandations existent au niveau européen et au niveau national. Un nombre conséquent de professionnels, 516 soignants (majoritairement des médecins, puis des infirmiers, et enfin des sages-femmes) ont répondu au questionnaire d’identification des freins. Un tiers de ces professionnels n’identifie pas de frein au respect de la procédure de nettoyage et de désinfection des SEE. Les deux autres tiers de ces professionnels verbalisent un manque de formation à la technique, un manque de matériel ou d’information sur la procédure. Le traitement et la désinfection des sondes SEE ne semblent pas être abordés dans les études médicales. On peut rapprocher cette enquête sur les freins et l’étude d’Andolfo [32], qui identifie aussi des freins à l’utilisation de solution hydro-alcoolique dans un service d’urgence, et qui considère que ce travail constitue une base théorique permettant d’engager le dialogue avec tous les professionnels potentiellement « fâchés » avec les pratiques d’hygiène.
Conclusion
Malgré une faible participation des établissements de santé de la plupart des régions françaises, variable selon les régions, cet audit observationnel des pratiques de nettoyage et de désinfection des sondes d’échographie endocavitaires a permis de recueillir 926 observations. L’analyse de ces résultats parfois hétérogènes pour les mêmes étapes du processus de désinfection de niveau intermédiaire a permis de constater qu’il existait encore de nombreux axes d’amélioration à mettre en œuvre pour atteindre les objectifs fixés par les recommandations nationales. Cette nouvelle enquête continue d’interroger les experts de la gestion du risque infectieux qui composent les CPias et l’inter-CPias quant à l’appropriation des recommandations nationales relatives à la prévention du risque infectieux associé aux actes utilisant des SEE publiées en 2019, ainsi que des recommandations de la SF2H relatives au traitement des dispositifs médicaux réutilisables publiées en 2022. En parallèle de cet audit, des fiches d’information avaient été conçues, publiées et diffusées par l’inter-CPias afin d’apporter une aide aux professionnels dans les étapes de désinfection des sondes, quelle que soit la méthode. Cela semble ne pas avoir suffi. De même, les réponses apportées au questionnaire sur les freins confirment le besoin urgent de repréciser ces recommandations et de renforcer la formation des professionnels de santé acteurs dans ce domaine. Par conséquent, après avoir mené deux enquêtes nationales en 2022 puis en 2023, et dans la perspective d’une amélioration des pratiques professionnelles associées aux actes utilisant les SEE, l’inter-CPias a informé la SF2H des résultats de ce dernier quick audit, par une première présentation des résultats au cours du congrès national SF2H de 2024, et par l’envoi du rapport à son président. L’inter-CPias espère que cette sollicitation suscitera une nouvelle réflexion de la part du conseil scientifique de la SF2H pour améliorer l’acquisition des recommandations relatives à la prévention du risque infectieux associé aux actes utilisant les SEE par les professionnels. L’inter-CPias a également proposé de communiquer les résultats de cet audit en adressant un courrier aux différents Ordres nationaux, des obstétriciens et gynécologues, des collèges d’échographie fœtale, et des sages-femmes, concernés par une pratique quotidienne de ces actes à risque infectieux. Enfin, et dans l’attente d’un retour du conseil scientifique de la SF2H, le groupe inter-CPias réfléchit déjà à de nouveaux outils pour répondre aux besoins de formation et d’information sur l’entretien des SEE (kits de formation, fiches d’information sur le choix des lingettes, etc.) en complément de ceux déjà proposés (Annexe I), ainsi qu’à la promotion d’un nouvel outil de visite de risques visant à sécuriser les actes en échographie endovaginale, diffusé par le CPias Nouvelle-Aquitaine en 2024.
Notes :
1- Virus de l’hépatite C et virus de l’immunodéficience humaine.
2- Human papillomavirus, virus du papillome humain.
3- Accessible à : https://sante.gouv.fr/IMG/pdf/note_d_information_ars_see_19_juillet_2019.pdf (Consulté le 30-01-2025).
4- Guide de bonnes pratiques de traitement des dispositifs médicaux réutilisables. Hygiènes. 2022;30(5):92 p. Accessible à : https://www.sf2h.net/publications/guide-de-bonnes-pratiques-de-traitement-des-dispositifs-medicaux-reutilisables.html (Consulté le 17-01-2025).